Современные подходы к вакцинопрофилактике гриппа.
Караулов А.B., Евсегнеева И.В. Дата публикации на сайте: 2011-11-09 Доступна также в печатной версии журнала Резюме | Полный текст | Скачать в PDF
Контакт: drkaraulov@mail.ru (495)118-50-47
Резюме:
Как известно, грипп способен чрезвычайно быстро распространяться в виде эпидемий и пандемий. Периодичность эпидемий связана с частым естественным изменением антигенной структуры вируса. В 2011 году в России заболеваемость гриппом и ОРВИ на 20-30% ниже по сравнению с 2009 и 2010 гг., при этом преобладающим является штамм H1N1. Признано, что единственным эффективным способом борьбы с гриппом является вакцинопрофилактика. Однако, в настоящее время в России охват прививками против гриппа хотя и имеет тенденцию к увеличению, но остается на уровне, который неспособен оказать существенное влияние на эпидемический процесс. Между тем, в исследованиях последних лет доказана важность создания «иммунной прослойки» для снижения общей заболеваемости в коллективах. Необходимо отдавать предпочтение вакцинам последнего поколения, т.к. они имеют наилучший профиль эффективности и безопасности. Так, в ходе клинических испытаний инактивированной полимер-субъединичной вакцины IV поколения «Гриппол® плюс» с участием различных контингентов населения были убедительно продемонстрированы ее высокая безопасность и противоэпидемическая эффективность.
Ключевые слова: грипп, эпидемия, вакцинопрофилактика, полимер субъединичная вакцина
ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздравсоцразвития России
Заболеваемость гриппом остается актуальной проблемой для здравоохранения. Как известно, гриппом принято считать острое инфекционное заболевание дыхательных путей, вызываемое вирусом гриппа и входящее в группу острых респираторных вирусных инфекций (ОРВИ). Нередко пациенты и ряд врачей называют гриппом любое острое респираторное заболевание (ОРВИ), однако кроме гриппа на сегодняшний день описано еще более 200 видов других респираторных вирусов (аденовирусы, риновирусы, респираторно-синцитиальные вирусы и др.), вызывающих заболевания со схожими симптомами [18].
Вирус гриппа имеет форму шара диаметром 80-120 нм, в центре которого находятся РНК-фрагменты, заключенные в липопротеидную оболочку. На поверхности оболочки имеются «шипы» состоящие из гемагглютинина (H) и нейраминидазы (N). Антитела, вырабатываемые в ответ на гемагглютинин (H), составляют основу иммунитета против определенного подтипа возбудителя гриппа. В настоящее время выявлено уже более 2000 вариантов вируса гриппа, которые имеют различия в антигенном спектре. Вирус гриппа относится к семейству Ortomyxoviridae, которое включает роды Influenza A, B и С. Антигенные свойства внутренних белков вириона (M1 и NP) определяют принадлежность вируса тому или иному роду [4,8]. Дальнейшее деление проводится согласно подтипам (серотипам) поверхностных белков гемагглютинина (HA) и нейраминидазы (NA). В соответствии с антигенной специфичностью поверхностных гликопротеидов HA и NA в настоящее время известно 16 подтипов HA и 9 подтипов нейраминидазы (NA) [4,9,23]. Эпидемическое значение для человека имеют вирусы, содержащие три подтипа HA (H1, H2 и H3) и два подтипа NA (N1 и N2). Вирусы гриппа А и В содержат NA и НА в качестве основных структурных и антигенных компонентов вирусных частиц, обладающих гемагглютинирующей и нейраминидазной активностями. У вируса гриппа С отсутствует нейраминидаза. Вместо нее вирус обладает гемагглютинин-эстеразным проникающим белком (HEF). Нить РНК окружена белком и упакована в липопротеидную мембрану. Вирионы способны агглютинировать эритроциты и элюироваться в них с помощью вирус-специфических ферментов [8]. Для вирусов сероварианта А (реже В) характерно частое изменение антигенной структуры при пребывании их в естественных условиях. Эти изменения определяют множество названий подтипов, которые включают место первичного появления, номер и год, когда вирус был выделен, а также характеристику HN: например A/Moscow/10/99 (H3N2); A/New Caledonia/120/99 (H1N1); B/Hong Kong/330/2001.
К гриппу восприимчивы все возрастные категории людей. Грипп характеризуется аэрозольным механизмом передачи (путем вдыхания мельчайших капель слюны, слизи и т.п., содержащих вирус гриппа) и чрезвычайно быстрым распространением в виде эпидемий и пандемий. Источником инфекции может-являться больной как с явной, так и со стёртой формами болезни, выделяющий вирус с кашлем, чиханием и т. д. Больной становится заразен с первых часов заболевания и остается таковым до 3-5-х суток развития заболевания. Попадая в системный кровоток из респираторных путей, вирус гриппа в первую очередь поражает сердечно-сосудистую систему и клетки крови. Кроме того, что вирус гриппа оказывает собственное токсическое воздействие, под его влиянием значительно ослабляются защитные иммунные механизмы, открывая ворота для бактериальной инфекции. Известно, что такие тяжелые клинические состояния, как вторичная пневмония, бронхит, осложнения со стороны нервной и сердечно-сосудистой системы, обострение хронических заболеваний (сахарный диабет, сердечная недостаточность, хронические обструктивные бронхопневмонии и т. д.) часто являются причиной отсроченной смерти, особенно у детей до 2-х лет, пожилых людей и лиц с ослабленным здоровьем [3,13]. В России смертность от гриппа последние годы остается весьма на высоком уровне [15] (см. таблицу 1).
Таблица 1. Статистика смертности от ОРВИ, включая грипп (по данным Минздравсоцразвития РФ).
Год | % летальных исходов от числа заболевших | Всего заболевших (данные статистической формы №1 Роспотребнадзора) | Количество летальных исходов (данные Росстата) |
2008 | 0,002 | 27 776 798 | 428 |
2009*** | 0,003 | 33 890 622 | 1302 |
2010 (11 месяцев) | 0,003 | 24 386 194 | 641 |
*** с августа 2009 года по январь 2010 года – пандемический грипп А Н1N1.
Эпидемии гриппа, вызванные серотипом А, возникают примерно каждые 2-3 года, а вызванные серотипом В — каждые 4-6 лет. Серотип С не вызывает эпидемий, только единичные вспышки у детей и ослабленных людей. Распространение гриппа в виде эпидемий встречается чаще в осенне-зимний период. Периодичность эпидемий связана с частым изменением антигенной структуры вируса при пребывании его в естественных условиях. Группами высокого риска считаются дети, люди преклонного возраста, беременные женщины, люди с хроническими болезнями сердца, легких, а также лица, страдающие хронической почечной недостаточностью [8,9,11].
Распространенность гриппа остается чрезвычайно высокой. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно во время сезонных эпидемий заболевает гриппом до 20% населения Земли, тяжелые формы отмечаются в 3–5 млн. случаев, а летальные исходы имеют место в 250–500 тыс. случаев [3]. На высокую заболеваемость гриппом оказывают влияние следующие факторы:
• воздушно-капельный путь передачи инфекции;
• способность вируса быстро меняться, преодолевая естественную иммунную защиту человека, приобретая резистентность к противовирусным препаратам;
• высокая плотность населения в странах Европы, Азии, США;
• глобализация, интенсивная миграция населения из страны в страну.
Свежими данными о распространенности гриппа в России располагают НИИ гриппа и НИИ вирусологии им. Д.И. Ивановского Минздравсоцразвития РФ, которые имеют 59 опорных баз во всех регионах страны. На опорных базах осуществляется постоянный эпидемиологический и этиологический мониторинг за гриппом и ОРВИ. В частности, оценивается эпидемический порог суммарной заболеваемости гриппом и ОРВИ – интенсивный показатель, который рассчитывается по многолетним данным по обращаемости населения за медицинской помощью для каждой недели и каждой возрастной группы населения города (всего населения). Данный показатель может разниться для каждого города. Превышение эпидемического порога на 20% и более в течение 2-х недель в совокупности с увеличением частоты диагностирования вирусов гриппа может говорить о начале эпидемии гриппа в конкретном городе [15].
В декабре 2010 года даже по завершении иммунизации против гриппа групп населения, относящихся к группам «риска», при неэпидемиологической обстановке в целом по стране в ряде регионов было зарегистрировано превышение эпидемического порога. В частности, в Екатеринбурге превышение эпидемического порога по населению в целом составило 40,3%, за счет превышения эпидемических порогов заболеваемости в детских возрастных группах на 46,9%, 31,5% и 35,2%. В Челябинске заболеваемость по населению в целом ниже эпидемического порога, но в детских возрастных группах пороги превышены на 25,3% – 31,5%. На Дальнем Востоке эпидемические пороги по населению в целом были незначительно превышены в Якутске (на 14,0%) и в Магадане (на 15,0%). В Якутске наблюдалось превышение порогов среди взрослого населения на 22,7% и детей школьного возраста на 20,9%, соответственно. В Магадане – среди детей школьного возраста на 34,9%. Кроме того, пороги превышены в одной из детских возрастных групп Ю. Сахалинска (0-2 лет – на 27,4%), Владивостока (3-6 лет – на 21,2%) и Хабаровска (7-14 лет – на 21,2%).
В Сибирском федеральном округе незначительно превышен порог в Иркутске (на 14,2% за счет заболеваемости лиц старше 15 лет), в г. Чита порог превышен только у детей 7-14 лет на 29,6%.
В Приволжском федеральном округе в Казани превышение порога по населению в целом на 18,1% связано с заболеваемостью детей 7-14 лет, у которых превышение порога составило 61,5%. Кроме того, в г. Чебоксары превышен порог у детей 0-2 лет на 32,2% и в Кирове у школьников на 17,5%.
В Северо-западном федеральном округе в Великом Новгороде превышен эпидемический порог на 17,7% за счет заболеваемости детей 3-6 лет (порог превышен на 25,5%).
В городах Центрального и Южного федеральных округов заболеваемость ниже эпидемических порогов по населению в целом и по отдельным возрастным группам, за исключением Воронежа, где небольшое превышение эпидемических порогов отмечено у детей 0-2 и 3-6 лет на 26,2% и 25,7%.
Таким образом, в целом в России на конец 2010 г. сохранялась неэпидемическая ситуация по гриппу. Спорадические случаи заболеваемости гриппом В выявлены в регионах Приволжского и Северо-западного федеральных округов, гриппом А(Н3N2) – в регионах Дальневосточного и Сибирского федеральных округов.
Последние доступные на момент написания статьи данные из вышеперечисленных источников свидетельствуют, что в начале 2011 года вновь зарегистрировано превышение эпидемических порогов заболеваемости по всему совокупному населению в 19 городах Российской Федерации, расположенных во всех федеральных округах:
• Дальневосточный (Биробиджан);
• Сибирский (Омск, Томск, Чита);
• Уральский (Екатеринбург, Челябинск);
• Приволжский (Нижний Новгород, Чебоксары, Оренбург, Самара);
• Центральный (Москва, Воронеж, Владимир, Рязань, Смоленск);
• Северо-Западный (Великий Новгород, Петрозаводск);
• Южный (Волгоград).
При этом в разных регионах страны превышение эпидемических порогов колебалось от 20,6% до 90,0%. Наиболее высокие показатели заболеваемости населения регистрировались в Нижнем Новгороде, Челябинске и Омске, где наряду с г. Москвой отмечено наибольшее число лабораторно подтвержденных случаев пандемического гриппа А/Н1N1.
Пандемический вирус гриппа А/H1N1 и вирус гриппа В выделялся у больных гриппом во всех субъектах Российской Федерации, в которых был превышен эпидемический порог заболеваемости.
Таким образом, пока в 2011 году регистрируется заболеваемость гриппом и ОРВИ на 20-30% ниже по сравнению с показателями 2009 и 2010 гг. В структуре заболеваемости гриппом и ОРВИ в России вирусы гриппа занимают порядка 10-15%. При этом среди вирусов гриппа преобладающим в текущем году является штамм H1N1, на который приходится около 40% в структуре заболеваемости.
По данным EuroFlu (Еженедельный электронный бюллетень) аналогичная ситуация имеет место и в странах Евросоюза. Грипп распространяется по странам Европы в направлении с запада на восток, лабораторно подтвержден у 44% заболевших. Доминирующее положение занимает вирус пандемического гриппа A(Н1N1) – 2009, по-прежнему поступают сообщения о случаях гриппа с тяжелым течением. На 3 неделе 2011 года в 3-х странах Евросоюза (Ирландия, Испания и Англия) активность гриппа достигала пиковых значений.
Экономическое бремя
В последние годы использование экономических показателей, оценивающих значимость инфекционных болезней и эффективность применяемых профилактических и противоэпидемических мероприятий стало необходимым условием результативной работы регуляторных органов и специалистов по рациональному фармацевтическому менеджменту в совершенствовании стратегии и тактики противоэпидемической деятельности [2,12]. Оценка данных показателей при инфекционных заболеваниях представляет определенные трудности вследствие постоянной изменчивости инфекционной патологии и формирующих ее факторов.
ФГУЗ «Центр гигиены и эпидемиологии в городе Москве» по Московскому региону оценивал средние взвешенные («стандартные») значения экономического ущерба на один случай для наиболее распространенных среди населения г. Москвы инфекционных болезней за 2010 год [12].
Экономические потери в связи с инфекционной заболеваемостью в расчете на один средний взвешенный случай были выбраны за основу экономического анализа. Эти величины используются в практике как в исходном виде (ущерб, значимость), так и в качестве важнейшего звена при расчетах экономической эффективности реализуемых профилактических, противоэпидемических и лечебных мероприятий. В ходе выполнения работы были проведены расчеты значения экономического ущерба на 1 случай заболевания и на совокупность случаев по 29 инфекционным болезням, зарегистрированным в Москве в 2010 г. В пересчете на один случай экономический ущерб от гриппа по сравнению с другими инфекционными заболеваниями невелик и составляет 17,1 тыс. руб. В то же время, он составляет, например, при менингококковой инфекции – 180,3 тыс. руб, бруцеллезе – 189,1 тыс. руб., а при тифопаратифозных инфекциях – 213,1 тыс. руб. (см. рисунок 1).
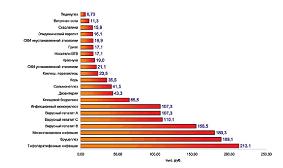 | Рисунок 1: Экономический ущерб на 1 случай заболевания некоторыми инфекционными болезнями в Москве в 2010 году. |
Однако за счет существенно большей распространенности ОРВИ в популяции, нежели распространенность других инфекционных заболеваний, воздушно-капельные инфекции вносят существенный вклад в суммарный экономический ущерб в г. Москве. Как и в предшествующие годы, наибольший экономический ущерб формируется распространением гриппа и ОРВИ – 26,7 млрд. руб. (см. таблицу 2). При исключении этой величины из состава совокупного ущерба на долю всех остальных инфекционных болезней приходится 3,5 млрд. руб.
Таблица 2. Динамика величин суммарного экономического ущерба (значимости) в Москве за период 2001-2010 гг. (млрд. руб.).
| Годы | Суммарный ущерб | В том числе от гриппа и ОРВИ | От прочих болезней | | 2001 | 4,2 | 3,5 | 0,7 | | 2002 | 5,4 | 4,5 | 0,9 | | 2003 | 9,9 | 9,0 | 0,9 | | 2004 | 12,1 | 10,6 | 1,5 | | 2005 | 11,7 | 10,1 | 1,6 | | 2006 | 15,2 | 13,3 | 1,9 | | 2007 | 19,6 | 17,1 | 2,5 | | 2008 | 20,5 | 17,8 | 2,7 | | 2009 | 32,1 | 29,4 | 2,7 | | 2010 | 30,2 | 26,7 | 3,5 |
Вакцинопрофилактика как эффективный способ борьбы с гриппом
Единственным социально и экономически эффективным способом борьбы с гриппом, по мнению ВОЗ, является вакцинопрофилактика [11,23]. Благодаря ежегодной вакцинации групп населения, относящихся к группам риска, в последние годы удалось существенно снизить интенсивность эпидемий гриппа во многих странах Евросоюза и в США. Органы здравоохранения стран Евросоюза (EMEA – European Medical Agency, Европейское медицинское агентство) и США (CDC – Centers of Disease Control, Центры по контролю за заболеваниями) подчеркивают целесообразность и обоснованность вакцинации против гриппа и прилагают усилия, направленные на увеличение охвата иммунизацией целевых групп до 75% [3,23].
В России с 1999 г. иммунизация против гриппа проводилась только по эпидемическим показаниям на региональном уровне. Т.к. закупка вакцин против гриппа являлась расходным обязательством субъектов РФ, охват населения оставался низким: так, в период осенней прививочной кампании 2005 г. было вакцинировано только 12% населения РФ [3]. В 2006 г. вакцинация против гриппа была включена в Национальный календарь профилактических прививок и стала расходным обязательством федерального бюджета, что повысило охват прививками населения (см. таблицу 3).
Таблица 3. Охват вакцинацией против гриппа населения Российской Федерации.
| Сезон | Численность привитых, млн. чел. | Доля привитого населения, % | | В рамках национального проекта «Здоровье» | Дополнительные источники | | 2006-2007 | 22,00 | 6,69 | 20,00 | | 2007-2008 | 25,08 | 6,13 | 21,91 | | 2008-2009 | 18,00 | 8,90 | 18,93 | | 2009-2010 | 27,40 | 7,00 | 24,00 | | 2010-2011 | 27,95 | 6,25 | 24,10 |
В 2010 г. иммунизацией против гриппа, проходившей в рамках приоритетного национального проекта «Здоровье», по данным органов управлений здравоохранения субъектов Российской Федерации, было охвачено свыше 26 млн. человек. В преддверие эпидсезона 2010-2011 гг. в строгом соответствии с заявками органов управления здравоохранением субъектов РФ Минздравсоцразвития закупило для иммунизации населения более 28 млн. доз вакцин против гриппа, в том числе вакцины «Гриппол® » для взрослых – более 16,9 млн. доз и вакцины «Гриппол® плюс» для детей дошкольного и школьного возраста – более 11,28 млн. доз. В состав вакцин были включены 3 актуальных штамма вируса гриппа, в том числе пандемический А/H1N1, А/H3N2 и В. Иммунизация населения против гриппа по данным органов управления здравоохранением субъектов Российской Федерации была завершена в декабре 2010 года. Всего было привито около 100% от числа подлежащих прививкам, в том числе – свыше 11 млн. детского населения и 16 млн. взрослого населения [3,14,15].
В 2009 году пандемия гриппа А/H1N1 как новый вызов человечеству заставила медицинское сообщество еще раз пересмотреть подходы к проблеме вакцинации против гриппа. Ситуация с пандемическим гриппом продиктовала необходимость органам здравоохранения государств в сотрудничестве с ВОЗ отработать систему быстрого реагирования на инфекционную угрозу. Так, благодаря информации, предоставленной ВОЗ о глобальном распространении гриппа А/H1N1, и разработке международных медико-санитарных правил, в Российской Федерации были своевременно предприняты все необходимые противоэпидемические меры. Российскими специалистами в максимально возможные кратчайшие сроки были разработаны, прошли полный цикл доклинических и клинических испытаний и получили разрешение к применению 4 вида вакцин против гриппа; проведена массовая иммунизация населения, относящегося к группам высокого риска. В рамках сотрудничества с ВОЗ была оказана консультационно-методическая помощь в разработке противогриппозных вакцин ученым Таиланда, Индии и ряда других стран. Создание российских эффективных противовирусных препаратов, к которым высоко чувствителен вирус гриппа А/Н1N1, позволило не только обеспечить население России своевременным и адекватным лечением, но и оказать гуманитарную помощь Украине [14].
Вместе с тем, из таблицы 3 видно, что охват прививками хотя и имеет тенденцию к увеличению, но остается на таком уровне, который неспособен оказать существенное влияние на эпидемический процесс при гриппе. Для эффективного контроля эпидемической ситуации необходимо вакцинировать не менее 50% населения [3,4]. Увеличение «иммунной прослойки» представляется возможным за счет включения новых контингентов и групп населения, в т.ч. здорового работоспособного населения.
Сегодня основным фактором, определяющим отказ от вакцинации против гриппа, является недостаточная информированность и боязнь вакцинации. Известно, что при вакцинации школьников значительная часть отказов от прививок приходится на долю часто болеющих детей и детей с хроническими заболеваниями, в то время как именно такой группе населения вакцинация против гриппа показана в первую очередь. Залогом успешной реализации региональной программы вакцинопрофилактики гриппа служат [3]:
• повышение уровня информированности о пользе иммунизации среди лиц, формирующих политику и принимающих решения на всех уровнях, для обеспечения постоянной поддержки и внимания к вопросам иммунизации;
• постоянно функционирующая система образовательных программ для населения на всех уровнях;
• поддержка губернатора и правительства региона, активная позиция руководства учреждений здравоохранения;
• грамотность медицинских работников в вопросах вакцинопрофилактики;
• наличие сети вакцинальных кабинетов, оказывающих услуги населению по вакцинопрофилактике на бюджетной и хозрасчетной основе.
Региональным органам государственной власти также необходимо принять меры по увеличению объемов закупок вакцин с привлечением всех возможных источников финансирования для проведения иммунизации населения, не включенного в Национальный приоритетный проект “Здоровье”. Из табл. 1 видно, что использование препаратов, закупаемых за счет дополнительных источников, позволило повысить охват прививками до 24,1% [3,11].
Виды вакцин против гриппа
В настоящее время в России зарегистрировано свыше 20 вакцин против гриппа 4-х поколений. К I поколению относятся цельновирионные живые и инактивированные вакцины. Живые вакцины содержат частицы живого вируса, их применение на сегодняшний день ограничено. Инактивированные гриппозные вакцины I поколения содержат прошедшие инактивацию целые вирусы и обладают хорошими показателями иммуногенности и высокой реактогенностью. Ко II поколению относятся расщепленные вакцины (сплит-вакцины), содержащие частицы разрушенного вируса, гемагглютинин, нейраминидазу и внутренние белки (по 15 мкг гемагглютинина каждого штамма вируса гриппа, входящего в вакцину, реактогенные липопротеиды и внутренние белки). Вакцины III поколения (субъединичные вакцины) содержат высокоочищенные поверхностные белки (гемагглютинин и нейраминидазу) которые наиболее важны для индукции иммунного ответа против гриппа (по 15 мкг антигенов вируса) и обладают хорошими показателями иммуногенности и безопасности. Остальные белки вириона и куриного эмбриона удаляются при очистке. К IV поколению вакцин против гриппа относят субъединичные адъювантные вакцины, которые содержат кроме высокоочищенных поверхностных белков еще и адъювант – вещество, используемое для усиления иммунного ответа при введении одновременно с иммуногеном. Использование адъюванта позволяет уменьшить содержание антигенов до 5 мкг на каждый штамм, сохранив высокие показатели иммуногенности и безопасности для всех контингентов [3,9,11,17]. Т.к. все вакцины производятся из штаммов вирусов гриппа, ежегодно рекомендуемых ВОЗ, при схожей эффективности вакцины против гриппа имеют весьма различающийся профиль безопасности, обусловленный различиями в составе препаратов.
Современные инактивированные гриппозные вакцины последнего поколения относятся к наиболее высокотехнологичным биологическим препаратам. В России разработана вакцина «Гриппол® плюс», которая относится к последнему, IV поколению вакцин против гриппа. Вакцина «Гриппол® плюс» в качестве адъюванта содержит иммуномодулятор «Полиоксидоний», благодаря чему стало возможным уменьшить содержание вирусных антигенов в три раза (до 5 мкг) по сравнению с зарубежными вакцинами против гриппа. Вакцина не содержит консервантов и антибиотиков и выпускается в современной упаковке (шприц-доза). «Гриппол® плюс» одобрен регуляторными органами РФ для массовой иммунопрофилактики гриппа у детей с 3-х лет, подростков и взрослых без ограничения возраста [3,6]. В настоящее время завершается процесс регистрации этой вакцины для применения у детей, начиная с 6-месячного возраста.
Следует отметить, что на сегодняшний день в отношении эффективности и безопасности вакцины «Гриппол® плюс» имеется солидная объективная доказательная база. В последние годы были опубликованы результаты предрегистрационных и пострегистрационных клинических исследований, проведенных в соответствии с международными стандартами (многоцентровые плацебо-контролируемые двойные-слепые сравнительные клинические исследования). В них оценивались иммуногенность и безопасность вакцины у здоровых взрослых и детей, а также у особых контингентов – больных с хроническими обструктивными заболеваниями легких и беременных женщин.
Безопасность и иммуногенность вакцины «Гриппол® плюс» при вакцинации здоровых взрослых была подтверждена в двойном слепом закрытом рандомизированном сравнительном контролируемоом клиническом исследовании в параллельных группах [5,11]. В исследовании принимали участие 300 здоровых взрослых мужчин и женщин в возрасте 18–55 лет. В качестве препарата сравнения была взята вакцина «Гриппол®». Безопасность вакцины «Гриппол® плюс» оценивалась путем анализа количества и выраженности общих реакций. Бессимптомное течение вакцинального процесса было зарегистрировано у 95% получивших вакцину. Слабо выраженные вакцинальные реакции отмечались в 5% случаев, что сравнимо с результатами применения иных гриппозных субъединичных вакцин. У 3,1% получивших вакцину регистрировали местные реакции в виде небольшой гиперемии и болезненности в месте инъекции, которые сохранялись до 2-х суток после иммунизации. Сильных общих реакций на вакцинацию и поствакцинальных осложнений зарегистрировано не было [16]. Иммуногенность вакцины определяли накануне и через 21 день после вакцинации серологическим методом по методике, рекомендованной в Руководстве по гармонизации требований к противогриппозным вакцинам Европейского комитета по патентованным лекарственным препаратам (СPMP/BWP/214/96) [21]. Среди исходно серонегативных вакцинированных количество лиц с четырехкратной сероконверсией после вакцинации составило 73,5–89,1% для трех вакцинных штаммов; кратность нарастания титров для штаммов А(H1N1), A(H3N2) и В составила 15,9; 6,7 и 8,1, соответственно; уровень серопротекции — 76–95% [5,11]. Таким образом, результаты клинических исследований вакцины «Гриппол® плюс» у взрослых продемонстрировали ее высокую иммуногенность, безопасность и хорошую переносимость.
Сравнимые показатели эффективности и безопасности были получены и при иммунизации детей и подростков в возрасте от 3 до 17 лет. Оценку реактогенности вакцины «Гриппол® плюс» проводили на базе НИИ детских инфекций (г. Санкт-Петербург) с участием 153 детей указанного возраста, которых наблюдали в течение 5 дней после вакцинации [11,17]. Местные реакции (болезненность, гиперемия и уплотнение в месте введения непосредственно после вакцинации) наблюдались у 13,1 % привитых. Субъективные жалобы на болезненность в месте инъекции предъявляли только дети 7–17 лет. У детей от 3 до 6 лет чаще регистрировали объективные местные реакции: умеренная гиперемия и уплотнение в первые 2 суток после вакцинации. Жалобы на болезненность у данной возрастной группы, как правило, отсутствовали. Размеры гиперемии и уплотнения, в основном, не превышали 3–6 мм, у трех детей размер гиперемии составил, соответственно, 10; 20 и 30 мм, у одного ребенка зарегистрировано уплотнение до 15 мм. Все наблюдаемые явления в месте введения вакцины были расценены как нормальные реакции слабой степени выраженности. Они не вызывали дискомфорта и самостоятельно исчезали в течение 2–4 дней после инъекции вакцины. Системные реакции в виде головной боли и недомогания, боли в животе, нарушения сна отмечались в 2,6-6,3 % случаев только у детей старше 6 лет. Это позволяет предположить связь перечисленных системных реакций с учебной, физической нагрузкой и прочими факторами помимо иммунизации против гриппа. В целом, анализ безопасности вакцины «Гриппол® плюс» у детей и подростков показал хорошую переносимость. Нежелательные явления наблюдались у небольшого числа привитых и относились к нормальным реакциям слабой степени выраженности. Авторы исследования постулируют, что вакцина «Гриппол® плюс» является слабореактогенным препаратом с высоким уровнем безопасности и может быть рекомендована для широкого применения в детской практике, в т.ч. в рамках Национального календаря прививок.
Еще одним интересным исследованием эффективности вакцины «Гриппол® плюс» у детей было предпринятое в 2008-2009 гг. изучение противоэпидемической эффективности при вакцинации организованных коллективов школьников [10]. Данное проспективное открытое исследование проводились в 9 школах г. Подольск Московской обл. и г. Санкт-Петербург в период подъема заболеваемости ОРВИ. В исследовании приняли участие 3203 ребенка возрасте 7–15 лет. Контрольную группу составляли 1253 здоровых ребенка, от родителей которых не было получено согласия на вакцинацию в соответствии с законом. В основную группу вошли 1950 здоровых детей, которые не имели противопоказаний к вакцинации и чьи родители подписали формализованное информированное согласие. При начале острого инфекционного процесса для подтверждения клинического диагноза «грипп» у детей обоих групп производилось выборочное вирусологическое исследование носоглоточных смывов. Анализ заболеваемости гриппом и ОРВИ в течение 6 месяцев после иммунизации подтвердил, что вакцина «Гриппол® плюс» обладает высокой противоэпидемической эффективностью, что проявляется в снижении заболеваемости гриппом привитых детей в 4,7 раза по сравнению с непривитыми, а другими ОРВИ – в 1,4 раза. Индекс противоэпидемической эффективности вакцины составил 4,7%, коэффициент противоэпидемической эффективности – 78,7%.
Другое исследование с участием 2768 здоровых детей в возрасте 7–17 лет проводилось в 5 школах г. Санкт-Петербурга. Контрольную группу составляли 1766 детей, которые на момент вакцинации были здоровы и не имели противопоказаний, но от родителей которых не было получено согласия на вакцинацию [7,11]. Охват прививками по школам составил в среднем 36,1%, варьируя по школам от 26,0% до 45,5%. Заболеваемость оценивали в течение 6 месяцев после иммунизации с использованием выборочной серологической верификации клинических диагнозов. Также оценивались продолжительность, степень тяжести и количество осложнений у заболевших в основной и контрольной группах. В ходе исследования было показано, что вакцина «Гриппол® плюс» обладает высоким профилем безопасности и хорошо переносится: выраженных общих и местных поствакцинальных реакций и осложнений зарегистрировано не было. Анализ тяжести течения заболевания среди привитых и непривитых выявил, что частота случаев заболеваний средней тяжести у привитых детей составила 8,6%, что статистически достоверно ниже по сравнению с группой непривитых, где данный показатель составил 21,3%. Причем различие в показателях было более выражено у учеников начальной школы (1–4 классы) (7,3% и 24,3 % среди привитых и непривитых, соответственно). Кроме этого, иммунизация вакциной «Гриппол® плюс» способствовала уменьшению числа осложнений ОРЗ в 2,5 раза по сравнению с таковыми в группе непривитых [7].
Данные вышеперечисленных клинических испытаний убедительно подтверждают высокую эффективность и безопасность вакцины «Гриппол® плюс» у здоровых взрослых и детей.
Недавно были завершены и исследования безопасности и эффективности вакцины «Гриппол® плюс» у особых контингентов. Так, специалистами НИИВС им. И. И. Мечникова и ФГУ «НИИ пульмонологии» ФМБА России (г. Москва) было предпринято исследование безопасности, переносимости и профилактической эффективности вакцины у пациентов с такими пульмонологическими заболеваниями, как бронхиальная астма, хроническая обструктивная болезнь легких, бронхоэктатическая болезнь [7]. В исследовании принимали участие 65 пациентов. Все участники находились в периоде ремиссии, им проводилась необходимая базисная терапия. Вакцина «Гриппол® плюс» хорошо переносилась и не приводила к обострению основного заболевания. Умеренные местные реакции (покраснение, болезненность и уплотнение в месте введения) наблюдались у 4,6% пациентов. Общие реакции (субфебрильная температура, недомогание, головная боль) были отмечены у 12,3%. Все нежелательные явления имели легкий характер и проходили самостоятельно без медикаментозного вмешательства. У тех пациентов, которые были вакцинированы, в течение 6 месяцев частота ОРЗ снижалась в 1,4 раза, частота обострений бронхообструктивного синдрома – в 2,5 раза, частота амбулаторных визитов к врачу по поводу ОРЗ или обострения основного заболевания – более чем в 2 раза, потребность в стационарной помощи – в 3,9 раза. Следует отметить, что и у одного пациента не усилилась степень тяжести основного заболевания. Также было отмечено снижение потребности в антибиотиках, а у двух пациентов было принято решение полностью отменить системные глюкокортикостероды [11,19].
Опубликованные в 2011 г. результаты исследования вакцинации против гриппа беременных женщин также представляют особый интерес. Плацебо-контролируемое исследование проводилось с участием 91 беременной. Исследовались полимер-субъединичная вакцина «Гриппол® плюс», субъединичнаявакцина зарубежного производства и плацебо [20]. В обеих группах в зоне инъекции наблюдались умеренно выраженные местные реакции в виде боли и уплотнения мягких тканей, самостоятельно разрешившиеся в течение 2-3 дней после вакцинации. В частности, гиперемия в зоне инъекции наблюдалась у 14,28% вакцинированных «Гриппол® плюс». В позднем вакцинальном периоде местных изменений не регистрировалось. Общие реакции в группе вакцинированных как вакциной «Гриппол® плюс», так и зарубежной вакциной, были слабыми и встречались реже, чем в группе плацебо (p<0,05). Вакцинация не влияла на уровень общей заболеваемости и на общее самочувствие беременных женщин. Проведенное наблюдение позволило выявить, что клиническая переносимость беременными женщинами вакцины «Гриппол® плюс» сопоставима с таковой субъединичной вакцины зарубежного производства как по частоте местных, так и общих реакций. Полученные данные подтверждают возможность расширения практики использования вакцины «Гриппол® плюс» у беременных с минимальным риском развития нежелательных поствакцинальных реакций [11,20].
Отдельно хочется подчеркнуть необходимость создания иммунной прослойки для эффективной борьбы с эпидемиями гриппа. Иммунная прослойка – количественный показатель, представляющий собой выраженную в процентах долю населения, обладающую иммунитетом к той или иной инфекционной болезни. Если заразившийся гриппом человек попадает в коллектив, то чем больше привитых в этом коллективе, тем меньше вероятность прогрессивного распространения заболевания. Следовательно, чем выше доля привитых в коллективе, тем меньше путей для передачи вируса. Считается, что в коллективе, где иммунная прослойка стремится к 100%, заболеваемость гриппом снижается в 12 раз, к 50% –в 4,4 раза. В исследовании, посвященном оценке противоэпидемической эффективности вакцинации детей организованных коллективов и включавшем 4751 ребенка, было показано, что при охвате прививками 88,6–97,5% школьных коллективов коэффициент эффективности противогриппозных вакцин составил 85,6–98,4%, а индекс 12,2–39,0. Т.е. вакцинация снижала заболеваемость гриппом и ОРВИ привитых детей в среднем в 16,9 раз, коэффициент эффективности составил 94% [1].
В другом исследовании, проведенном под руководством Т.Н. Ильиной [10] подтверждена важность создания «иммунной прослойки» для снижения общей заболеваемости в коллективах: в тех школах, где охват вакцинацией против гриппа составил >60%, общий уровень заболеваемости ОРВИ (число заболевших на 1 тыс. чел.) был на 40% ниже по сравнению со школами с охватом <60% [17]. В исследовании Ерофеевой с соавт. показатели противоэпидемической защиты – индекс и коэффициент (К и Е) – составили 2,5 и 59,8, соответственно, при среднем охвате школьных коллективов вакцинацией 36,1%, что также подтверждает важность создания достаточной иммунной прослойки в коллективе. В других независимых исследованиях было показано, что вакцинация, помимо противоэпидемической защиты против гриппа, также снижала общую заболеваемость респираторными инфекциями в 1,4 раза [7,11].
Таким образом, результаты исследований вакцины «Гриппол® плюс» наряду с доказанной высокой безопасностью и противоэпидемической эффективностью подтверждают и целесообразность массовой вакцинопрофилактики коллективов для снижения общей заболеваемости.
Подводя резюме, хочется еще раз отметить способность гриппа чрезвычайно быстро распространяться в виде эпидемий и пандемий благодаря аэрозольному механизму передачи. Периодичность эпидемий связана с частым естественным изменением антигенной структуры вируса. Так, эпидемии гриппа, вызванные серотипом А, возникают примерно каждые 2-3 года, а вызванные серотипом В — каждые 4-6 лет. При этом дети, пожилые люди, беременные женщины, лица, имеющие хронические болезни сердца, легких и других внутренних органов считаются группами высокого риска. В 2011 году в России заболеваемость гриппом и ОРВИ на 20-30% ниже по сравнению с 2009 и 2010 гг., при этом преобладающим является штамм А/H1N1. За счет большой распространенности в популяции ОРВИ вносят существенный вклад в суммарный экономический ущерб. Единственным социально и экономически эффективным способом борьбы с гриппом, по мнению ВОЗ, является вакцинопрофилактика. Однако, в настоящее время охват прививками против гриппа хотя и имеет тенденцию к увеличению, но остается на уровне, который неспособен оказать существенное влияние на эпидемический процесс. Между тем, в исследованиях последних лет доказана важность создания «иммунной прослойки» для снижения общей заболеваемости в коллективах. Необходимо отдавать предпочтение вакцинам последнего поколения, т.к. они имеют наилучший профиль эффективности и безопасности. Так, в ходе клинических испытаний инактивированной полимер-субъединичной вакцины IV поколения «Гриппол® плюс» с участием различных контингентов населения были убедительно продемонстрированы ее высокая безопасность и противоэпидемическая эффективность.
Литература
1. Баташева И.И., Бурцев Д.В., Полякова Л.Л., Мельник Л.Н. Анализ медико-эпидемиологической эффективности вакцинопрофилактики гриппа среди детей организованных коллективов. Инфекционные болезни. 2010; 8(3): 72-76.
2. Белоусов Д.Ю., Куликов А.Ю., Колбин А.С., Карпов О.И., Быков А.В., Толкушин А.Г. Фармакоэкономика: зачем, где и как проводить фармакоэкономические исследования? Фармакоэкономика. 2010; 3(2): 19-21
3. Брико Н.И. Вакцинопрофилактика гриппа: успехи и перспективы. Безопасность медицинской деятельности. 2011; 9: 93-96
4. Букринская А.Г. Вирусология. Москва. 1986.
5. Войцеховская Е. М., Вакин В. С., Васильева А. А. и др. Результаты анализа иммуногенности новой гриппозной вакцины Гриппол® плюс. Эпидемиол. и вакцинопроф. 2009; 1 (44): 40–45.
6. Гриппол® плюс. Инструкция по медицинскому применению.
7. Ерофеева М. К., Никоноров И. Ю., Максакова В. Л. Оценка эффективности применения гриппозной вакцины Гриппол® плюс у детей школьного возраста в период эпидемии гриппа 2008–2009 г. Эпидемиол. и вакцинопроф. 2010; 3.
8. Жданов В.М., Гайдамович С.Я. Общая и частная вирусология, т. 1—2; М., 1982;
9. Жданов В.М., Львов Д.К. Эволюция возбудителей инфекционных болезней, М., 1984.
10. Ильина Т. Н. Оценка эпидемиологической эффективности гриппозной инактивированной полимер-субъединичной вакцины при иммунизации школьников//Вопр. современной педиатрии. 2009; 8(5): 48–52.
11. Костинов М.П., Ерофеева М.К., Харит С.М. Эффективность и безопасность вакцинопрофилактики гриппа у разных контингентов. Terra Medica. 2011; 2: 7-12.
12. О величине экономического ущерба от инфекционных заболеваний в Москве в 2010 году. ФГУЗ «Центр гигиены и эпидемиологии в городе Москве». Москва. 2011.
13. Семенов Б.Ф. Концепция отложенной смерти при гриппе и тактика вакцинопрофилактики инфарктов, инсультов и летальных исходов при этой инфекции. Российский Медицинский Журнал. 2003; 11(22).
14. Сквоцова В.И. Выступление на 63-ой сессии Всемирной ассамблеи здравоохранения в Женеве. 17 мая 2010 г.
15. Справка по ситуации с заболеваемостью гриппом и острыми респираторными вирусными инфекциями в Российской Федерации. Минздравсоцразвития РФ. 2011. Доступно на 12.08.2011: http://www.minzdravsoc.ru/health/flu/37
16. Харит С. М., Лиознов Д. А., Николаенко С. Л. Оценка реактогенности и безопасности вакцины гриппозной тривалентной инактивированной полимер-субъединичной «Гриппол® плюс» // В сб.: Материалы научно-практической конференции «Вакцинология-2008. Совершенствование иммунобиологических средств профилактики, диагностики и лечения инфекционных болезней» М., 11–12 ноября 2008.
17. Харит С. М., Начарова Е. П., Черняева Т. В. Безопасность инактивированной полимер-субъединичной тривалентной гриппозной вакцины. Пострегистрационное наблюдение. Вопр. современной педиатрии. 2009; 4: 30–34.
18. Царев С.В., Хаитов М.Р. Роль респираторных вирусов при бронхиальной астме. Русский Медицинский Журнал. 2009; 17(2): 136-140.
19. Чебыкина А.В., Костинов М.П., Магаршак О.О. Оценка безопасности и эффективности вакцинации против гриппа. Эпидемиол. и вакцинопроф. 2010; 55(6): 50-54
20. Черданцев А. П. Изучение клинической безопасности вакцинации против гриппа у беременных. Мед. альманах. 2011; 4(17).
21. Concept Paper on the Revision of the CPMP/ BWP Note for Guidance on Harmonization of Requirements for Influenza Vaccines (CPMP/ BWP/214/96)./London, 31 May, 2001//CPMP/EWP/1045/01.
22. Global agenda on influenza. Weekly Epidemiological Report. 2002; 77.
23. The Weekly Epidemiological Record. WHO. 2005; 33: 277–288.
24. Webster R. G., Bean W. J., Gorman O. T. et al.// Microbiol. Rev. — 1992. — Vol. 56.
MODERN APPROACHES TO FLU VACCINE PROPHYLACTIC
Karaulov A.V., Evsegneeva I.V.
SEI HPE first MGMU named after I.M. Sechenov
Abstract: as is known, the flu can spread very quickly as epidemics and pandemics. Periodicity of epidemics related to the frequent native changes in the antigenic structure of the virus. In Russia the incidence of influenza and SARS in 2011 are 20-30% lower compared with 2009 and 2010 with H1N1 as predominant strain. It is well recognized that the only vaccination is effective way to prevent the flu. However, at present time in Russia coverage of vaccination against flu even though it has a tendency to increase, but remains at a level that is unable to have a significant impact on the epidemic process. Meanwhile, recent researches proved the importance of creating an «immune stratum» to reduce the overall incidence in groups. Vaccines of last generation are more acceptable because they have the best profile of efficacy and safety. Thus, in clinical trials of an inactivated polymer-subunit IV generation vaccine «Grippol plus» with the participation of different populations its high degree of safety and anti-epidemic effectiveness have been convincingly demonstrated.
Keywords: flu, epidemic, vaccine prophylactic, polymer-subunit vaccine. |
|